Betegtájékoztató
1. Milyen típusú gyógyszer a Thalidomide BMS és milyen betegségek esetén alkalmazható?
Milyen típusú gyógyszer a Thalidomide BMS?
A Thalidomide BMS a talidomid nevű hatóanyagot tartalmazza. Ez a gyógyszer az immunrendszer működésére ható gyógyszerek csoportjába tartozik.
Milyen betegségekre alkalmazható a Thalidomide BMS?
A Thalidomide BMS-t két másik gyógyszerrel, az úgynevezett "melfalánnal" és "prednizonnal" együtt alkalmazzák olyan felnőtt betegek kezelésére, akik mielóma multiplexben, a rák egyik típusában szenvednek. Olyan embereknél alkalmazzák, akiknél a közelmúltban állították fel a diagnózist, és akiknek korábban még nem írtak fel egyéb gyógyszert a mielóma multiplexre, és betöltötték a 65. életévüket, vagy akik 65 évesnél fiatalabbak, de nem kezelhetők nagy dózisú kemoterápiával, amelyet esetenként nagyon nehezen visel a szervezet.
Mi a mielóma multiplex?
A mielóma multiplex a rák egyik fajtája, amely bizonyos típusú fehérvérsejteket, az úgynevezett plazmasejteket érinti. Ezek a sejtek a csontvelőben gyűlnek össze, és szabályozatlanul osztódnak. Ez károsíthatja a csontot és a vesét. A mielóma multiplex általában gyógyíthatatlan. A panaszokat és tüneteket azonban egy időre nagymértékben mérsékelni lehet vagy meg lehet szüntetni. Ezt nevezzük "remissziónak".
Hogyan hat a Thalidomide BMS?
A Thalidomide BMS a szervezet immunrendszerére gyakorol hatást, és közvetlenül a rákot támadja meg. Többféle módon fejti ki hatását:
- a rákos sejtek fejlődésének leállításával,
- az erek daganatban való növekedésének leállításával,
- az immunrendszer egy részének serkentésével, hogy az megtámadja a rákos sejteket.
2. Tudnivalók a Thalidomide BMS szedése előtt
Kezelőorvosa konkrét útmutatásokkal látja el Önt, különösen a talidomid magzatra gyakorolt hatásait illetően (ezt a Thalidomide BMS Terhességmegelőző Program ismerteti).
Kapni fog kezelőorvosától egy betegeknek szóló oktató brosúrát. Figyelmesen olvassa el, és tartsa be az ott található utasításokat.
Kérjük, hogy amennyiben nem teljesen érti ezeket az utasításokat, kérje meg kezelőorvosát, hogy magyarázza el újra, mielőtt elkezdené szedni a talidomidot. A további információkat lásd még ebben a pontban a "Figyelmeztetések és óvintézkedések" és a "Terhesség és szoptatás" cím alatt.
Ne szedje a Thalidomide BMS-t
- ha terhes, úgy gondolja, hogy terhes lehet, vagy terhességet tervez, mivel a Thalidomide BMS születési rendellenességeket és magzati halált okoz.
- ha fennáll a teherbe esés lehetősége, kivéve, ha hajlandó és képes betartani a szükséges fogamzásgátlási intézkedéseket a teherbeesés elkerülésére (lásd 2. pont, "Figyelmeztetések és óvintézkedések" és "Terhesség és szoptatás").
- ha teherbe eshet, kezelőorvosa minden újabb gyógyszerfelíráskor feljegyzi, hogy Ön minden szükséges óvintézkedést megtett, és erről Önnek is ad egy igazolást.
- ha allergiás a talidomidra vagy a gyógyszer ("A csomagolás tartalma és egyéb információk" című, 6. pontban felsorolt) egyéb összetevőjére.
Ne szedje a Thalidomide BMS-t, ha a fentiek bármelyike vonatkozik Önre. Ha nem biztos benne, beszélje meg kezelőorvosával vagy gyógyszerészével, mielőtt a Thalidomide BMS szedését megkezdené.
Figyelmeztetések és óvintézkedések
A következő esetekben a gyógyszer szedése előtt beszéljen kezelőorvosával, gyógyszerészével vagy a gondozását végző egészségügyi szakemberrel:
Thalidomide BMS-t szedő nőbetegek esetében
A kezelés megkezdése előtt kérdezze meg kezelőorvosát, hogy Ön teherbe eshet-e, még akkor is, ha úgy gondolja, hogy ez nem valószínű. Még ha a rák kezelését követően nincs is menstruációja, akkor is teherbe eshet.
Ha Ön teherbe eshet:
- Orvosa gondoskodni fog róla, hogy terhességi tesztet végezzenek Önnél
-- a kezelés megkezdése előtt
-- a kezelés során 4 hetente
-- a kezelés befejeződése után 4 héttel.
- Hatékony fogamzásgátló módszert kell alkalmaznia:
-- a kezelés megkezdését megelőző legalább 4 hét során
-- a kezelés alatt
-- a kezelés befejeződését követően legalább 4 hétig.
Orvosa elmondja Önnek, hogy milyen fogamzásgátló módszert alkalmazzon.
Ha Ön teherbe eshet, akkor kezelőorvosa valamennyi gyógyszerfelírás alkalmával rögzíti, hogy a fent leírtak szerint szükséges eljárások elvégzésre kerültek.
Thalidomide BMS-t szedő férfibetegek esetében
A Thalidomide BMS bejut az ondóváladékba, ezért tilos a védekezés nélküli közösülés, még akkor is, ha Ön vazektómián (vagyis mindkét ondóvezeték műtéti átvágásán) esett át.
- A terhességet, illetve a terhesség alatt a gyógyszerrel való mindennemű kapcsolatot el kell kerülni. Mindig használjon óvszert:
-- a kezelés alatt
-- a kezelés befejeződését követően legalább 7 napig.
- Nem adhat spermát:
-- a kezelés alatt
-- a kezelés befejeződését követően legalább 7 napig.
Minden beteg esetén
A Thalidomide BMS szedése előtt beszéljen kezelőorvosával:
- ha nem érti a kezelőorvosa által a fogamzásgátlásra vonatkozóan adott tanácsokat, vagy úgy érzi, hogy nem képes követni ezeket az útmutatásokat;
- ha szívrohama volt, valaha a múltban trombózisa volt (vérrög képződés), vagy amennyiben dohányzik, magas a vérnyomása vagy magas a koleszterinszintje. A Thalidomide-BMS-kezelés alatt megnő a vénákban és a verőerekben a vérrögök kialakulásának kockázata (lásd még: 4. pont "Lehetséges mellékhatások");
- ha korábban, vagy jelenleg is fennáll Önnél idegkárosodás (neuropátia), amely bizsergő érzést, koordinációs zavart vagy a kezekben, illetve lábakban érzett fájdalmat okoz (lásd még: 4. pont "Lehetséges mellékhatások");
- ha tapasztalt már, vagy jelenleg is fennáll Önnél lassú szívműködés (ez úgynevezett bradikardia tünete lehet);
- magas a vérnyomása a tüdőverőerekben (lásd még: 4. pont "Lehetséges mellékhatások");
- csökkent a fehérvérsejt száma (neutropénia), amit láz és fertőzés is kísér;
- csökkent a vérlemezke-száma. Ön hajlamosabb lesz vérzések és véraláfutások kialakulására;
- jelenleg májkárosodása (májbetegsége) van, vagy korábban volt, beleértve azt is, ha a májfunkciós vizsgálatok kóros eredményt mutattak;
- ha súlyos bőrreakciót, úgynevezett Stevens-Johnson-szindrómát, toxikus epidermális nekrolízist vagy DRESS szindrómát (más néven DRESS vagy gyógyszer-túlérzékenységi szindróma) tapasztal jelenleg vagy tapasztalt korábban. (A tünetek leírását lásd a "4. Lehetséges mellékhatások" című pontban);
- ha a talidomid szedése alatt allergiás reakciót észlelt, például bőrkiütést, viszketést, duzzanatot, szédülést vagy nehézlégzést;
- ha álmosságot tapasztal;
- ha lázat, hidegrázást és erős reszketést észlel, amely esetlegesen alacsony vérnyomással és zavartsággal járhat együtt (ezek súlyos fertőzések tünetei lehetnek);
- ha jelenleg vagy korábban bármikor vírusfertőzés állt fenn Önnél, különösen bárányhimlő, hepatitisz B fertőzés, HIV-fertőzés. Ha nem biztos ebben, beszéljen kezelőorvosával. A Thalidomide BMS-kezelés a vírust hordozó betegeknél a vírus ismételt aktiválódását eredményezheti, ami a fertőzés kiújulásához vezet. Kezelőorvosának ellenőriznie kell, hogy volt-e Önnek valaha hepatitisz B-fertőzése;
- ha vese- vagy májbetegsége van (lásd még: 4. pont "Lehetséges mellékhatások").
Lehetséges, hogy kezelőorvosa ellenőrizni fogja az Ön pajzsmirigyműködését a talidomid-kezelés megkezdése előtt és rendszeresen a kezelés alatt.
Azonnal számoljon be orvosának vagy az ellátását végző egészségügyi szakembernek, ha a kezelés alatt vagy azután bármikor: homályos látást, látásvesztést vagy kettős látást, beszédzavart, a kar vagy a láb gyengeségét, a járásában bekövetkező változást vagy egyensúlyproblémákat, hosszan tartó zsibbadást, csökkent érzékelést vagy érzéskiesést, emlékezetkiesést vagy zavartságot tapasztal. Ezek bármelyike tünete lehet a súlyos és akár halálos kimenetelű, progresszív multifokális enkefalopátiának (PML) nevezett, agyat érintő betegségnek. Amennyiben a fenti tünetek fennálltak Önnél az Thalidomide BMS-kezelés előtt, a tünetekkel kapcsolatos bármilyen változásról számoljon be orvosának.
Kezelőorvosa ellenőrizheti, hogy a daganat nagy mennyiségben van-e jelen a szervezetében, beleértve a csontvelőt is. Ez a daganatsejtek fokozott szétesését idézheti elő, ami kórosan megemelheti a szervezetében bizonyos kémiai anyagok szintjét, amelyek veseelégtelenséget okozhatnak (ezt az állapotot tumorlízisszindrómának nevezik) (lásd még: 4. pont "Lehetséges mellékhatások").
Kezelőorvosának meg kell vizsgálnia, hogy a Thalidomide BMS szedése során nem alakultak-e ki Önnél másfajta vérképzőszervi rosszindulatú betegségek (akut mieloid leukémia és mielodiszpláziás szindróma) (lásd még: 4. pont "Lehetséges mellékhatások").
A Thalidomide BMS el történő kezelés alatt és a kezelés befejeződését követően legalább 7 napig tilos vért adnia.
Ha nem biztos benne, hogy a fentiek bármelyike vonatkozik-e Önre, beszéljen kezelőorvosával, mielőtt megkezdené a Thalidomide BMS szedését.
Gyermekek és serdülők
A Thalidomide BMS alkalmazása gyermekek és 18 év alatti fiatalok esetében nem ajánlott.
Egyéb gyógyszerek és a Thalidomide BMS
Feltétlenül tájékoztassa kezelőorvosát vagygyógyszerészét a jelenleg vagy nemrégiben szedett egyéb gyógyszereiről, mivel más gyógyszerek befolyásolhatják a talidomid hatását. Ez vonatkozik a vény nélkül kapható gyógyszerekre, köztük a gyógynövénykészítményekre is.
Feltétlenül közölje kezelőorvosával, ha olyan gyógyszereket szed, amelyek:
- álmosságot okoznak, tekintve, hogy a talidomid fokozhatja ezek hatását. Ide tartoznak a nyugtatók (például szorongáscsökkentők, altatók, antipszichotikumok, H1-antihisztaminok, opiát származékok és barbiturátok);
- lassítják a szívműködést (lassú szívműködést, úgynevezett "bradikardiát" idéznek elő, például anti-kolinészterázok és béta-blokkolók);
- szívbetegségek és ezek szövődményeinek kezelésére szolgálnak (például digoxin) vagy vérhígítók (például warfarin);
- neuropátiát okozhatnak, például a rák ellen alkalmazható egyéb gyógyszerek;
- fogamzásgátlásra szolgálnak.
A ThalidomideBMS egyidejű bevétele étellel, itallal és alkohollal
Ne fogyasszon alkoholt, mialatt a Thalidomide BMS-t szedi. Ennek oka, hogy az alkohol álmosságot okoz, és a Thalidomide BMS-től még jobban elálmosodhat.
Terhesség és szoptatás
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége, vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
Terhesség
A talidomid súlyos születési rendellenességeket vagy magzati halált okoz.
- A terhesség alatt bevéve már egy kapszula is súlyos születési rendellenességet okozhat a magzatban.
- A fejlődési rendellenességek közé tartozik a karok vagy lábak megrövidülése, a kezek vagy a lábfejek torzulása, a szem vagy a fül fejlődési rendellenessége, illetve a belső szervekkel kapcsolatos problémák.
Ha Ön terhes, nem szedheti a Thalidomide BMS-t. Továbbá tilos teherbe esnie a Thalidomide BMS szedése alatt.
Amennyiben Ön teherbe eshet, legalább egy hatékony fogamzásgátló módszert kell alkalmaznia (lásd a "Tudnivalók a Thalidomide BMS szedése előtt" című 2. pontot).
Azonnal abba kell hagynia a kezelést, és értesítenie kell kezelőorvosát az alábbi esetekben:
- ha kimarad - vagy úgy véli, hogy kimaradt - egy menstruációs vérzése, szokatlan a menstruációs vérzése, vagy azt gyanítja, hogy terhes.
- ha heteroszexuális közösülésre került sor hatékony fogamzásgátló módszer alkalmazása nélkül. Ha a talidomid-kezelés során terhes lesz, azonnal abba kell hagynia a kezelést, és értesítenie kell kezelőorvosát.
Fogamzóképes női partnerrel rendelkező és Thalidomide BMS-t szedő férfibetegek esetében lásd a "Tudnivalók aThalidomide BMS szedése előtt" című 2. pontot. Ha a partnere terhes lesz, miközben Ön talidomidot szed, ezt azonnal jelentenie kell kezelőorvosának.
Szoptatás
Ne szoptasson, ha Thalidomide BMS-t szed, mivel nem ismert, hogy a talidomid bekerül-e az anyatejbe.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Amennyiben mellékhatásokat, például szédülést, fáradtságot, álmosságot vagy homályos látást észlel, ne vezessen gépjárművet és ne végezzen munkát gépekkel.
3. Hogyan kell szedni a Thalidomide BMS-t?
A Thalidomide BMS-t mindig a kezelőorvosa vagy gyógyszerésze által elmondottaknak megfelelően szedje. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Mennyit kell bevenni?
A készítmény ajánlott adagja napi 200 mg (4 × 50 mg-os kapszula) 75 éves és ennél fiatalabb betegek esetében, illetve vagy napi 100 mg (2 x 50 mg-os kapszula) 75 évesnél idősebb betegek esetében.
Azonban kezelőorvosa határozza majd meg az Ön adagját, és a betegség lefolyásának megfigyelése alapján módosíthatja is a dózist. Kezelőorvosa megmondja majd, hogyan és mennyi ideig kell a Thalidomide BMS-t szednie (lásd a "Tudnivalók a Thalidomide BMS szedése előtt" című 2. pontot).
A Thalidomide BMS szedése kezelési ciklusokban, naponta történik, mindegyik ciklus időtartama 6 hét. A gyógyszert melfalánnal és prednizonnal kombinációban kell szedni, amelyeket az egyes 6 hetes ciklusok 1-4. napján kell bevenni.
A gyógyszerszedésre vonatkozó útmutatások
- Ne törje össze, ne nyissa fel vagy rágja szét a kapszulákat! Ha a sérült Thalidomide BMS kapszulából származó por érintkezésbe kerül a bőrrel, azonnal alaposan le kell mosni szappannal és vízzel.
- Az egészségügyi szakembereknek, gondozóknak és családtagoknak eldobható kesztyűt kell viselniük a buborékcsomagolás, illetve a kapszula kezelésekor. Ezt követően a kesztyűt körültekintően kell levenni a bőrexpozíció elkerülése érdekében, majd lezárható műanyag polietilén zsákba kell helyezni és hulladékként kell kezelni a helyi előírásoknak megfelelően. Ezután pedig szappannal és vízzel alaposan kezet kell mosni. A várandós vagy vélhetően várandós nőknek tilos kezelniük a buborékcsomagolást vagy a kapszulát.
- A gyógyszert szájon át vegye be.
- A kapszulákat egészben, egy egész pohár vízzel vegye be.
- Ne törje össze, és ne rágja szét.
- Lefekvés előtt, egy adagban vegye be a kapszulákat, így napközben kisebb valószínűséggel fordul majd elő álmosság.
A kapszula buborékcsomagolásból történő eltávolításához a kapszulának csak az egyik végét nyomja ki a fólián keresztül. Ne nyomja meg a kapszula közepét, mert ez a kapszula törését okozhatja.
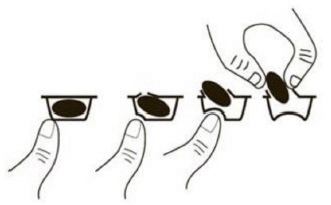
Ha az előírtnál több Thalidomide BMS-t vett be
Ha az előírtnál több Thalidomide BMS-t vett be, azonnal forduljon orvoshoz vagy menjen kórházba. Amennyiben lehetséges, vigye magával a gyógyszer dobozát és ezt a betegtájékoztatót is.
Ha elfelejtette bevenni a Thalidomide BMS-t
Ha elfelejtette bevenni a Thalidomide BMS-t a szokásos időben és
- 12 óránál rövidebb idő telt el, vegye be azonnal a kapszulát.
- 12 óránál hosszabb idő telt el, ne vegye be a kapszulát. Vegye be a következő kapszulát a következő napon a szokásos időben.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
A gyógyszer szedése során az alábbi mellékhatások fordulhatnak elő:
Hagyja abba a Thalidomide BMS szedését, és azonnal forduljon orvoshoz, ha a következő súlyos mellékhatásokat észleli, ugyanis sürgős orvosi kezelésre lehet szüksége:
- Rendkívül heves és súlyos bőrreakciók. A bőrön kialakuló mellékhatások hólyagos vagy hólyag nélküli kiütések formájában jelenhetnek meg. Kialakulhat bőrirritáció, fekélyek vagy duzzanatok a szájüregben, a torokban, a szemeken, az orron és a nemi szervek körül, valamint ödéma, láz és influenzaszerű tünetek. Ezek a tünetek ritka és súlyos bőrreakciók - Stevens-Johnson-szindróma, toxikus epidermális nekrolízis vagy DRESS-szindróma - jelei lehetnek.
- Allergiás reakciók, például helyi, illetve egész testre kiterjedő viszkető kiütések, angioödéma és anafilaxiás reakció (az allergiás reakciók súlyos típusai, amelyek csalánkiütés, bőrkiütés, a szem, a száj vagy az arc megduzzadása, nehézlégzés vagy viszketés formájában jelentkezhetnek).
Haladéktalanul tájékoztassa kezelőorvosát, ha a következő súlyos mellékhatások bármelyikét észleli:
- Zsibbadás, bizsergés, koordinációs zavarok vagy fájdalom a kézben vagy a lábfejben. Ennek oka idegkárosodás lehet (melyet "perifériás neuropátiának" nevezünk), amely nagyon gyakori mellékhatás. Ez lehet nagyon súlyos, fájdalmas, és munkaképtelenséget is okozhat. Ha ilyen tüneteket tapasztal, kérjük, azonnal forduljon kezelőorvosához, aki csökkentheti az adagot, vagy abbahagyathatja Önnel a kezelést. Ez a mellékhatás általában hónapokon át tartó gyógyszerszedés után lép fel, de ennél hamarabb, vagy valamivel a kezelés abbahagyása után is jelentkezhet. Előfordulhat, hogy nem, vagy csak lassan múlik el.
- Hirtelen mellkasi fájdalom vagy nehézlégzés.
Okozhatják a tüdőhöz vezető verőerekbe került vérrögök (ezt "tüdőembóliának" nevezzük), amely gyakori mellékhatás. Ez felléphet a kezelés ideje alatt, vagy a kezelés abbahagyása után is.
- Fájdalom vagy duzzanat a lábakban, különösen a lábszárban vagy a vádliban. Okozhatják a láb vénáiban keletkezett vérrögök (ezt "mélyvénás trombózisnak" nevezzük), amely gyakori mellékhatás. Felléphet a kezelés ideje alatt, vagy a kezelés abbahagyása után is.
- A karokba, nyakba, állkapocsba, hátba vagy gyomorba kisugárzó mellkasi fájdalom, verejtékezés és légszomj, hányinger vagy hányás.
Ezek szívroham/miokardiális infarktus tünetei lehetnek (amit a szívet ellátó verőerekben lévő vérrögök okozhatnak).
- Ideiglenes látás- vagy beszédzavar.
Ezek szélütés tünetei lehetnek (amit az agyat ellátó verőérbe került vérrög okozhat).
- Láz, hidegrázás, torokfájás, köhögés, fekélyek a szájban, illetve a gyulladás egyéb tünetei.
- Vérzések vagy véraláfutások kialakulása sérülés nélkül. Egyéb mellékhatások:
Fontos figyelembe venni, hogy néhány mieloma multiplexes betegnél kialakulhatnak egyéb típusú daganatos betegségek, különösen vérképzőszervi rosszindulatú betegségek, és ennek kockázatát a Thalidomide BMS kezelés növelheti. Emiatt kezelőorvosának alaposan értékelnie kell az előny és kockázat arányát, amikor Thalidomide BMS-t ír fel Önnek.
Nagyon gyakori mellékhatások (10 beteg közül több mint 1 betegnél fordulhatnak elő):
- székrekedés,
- szédülés,
- álmosság, fáradtság,
- reszketés (tremor),
- csökkent vagy rendellenes érzékelés (dizesztézia),
- a kezek és a lábfejek dagadása,
- a vérsejtek számának csökkenése. Ez jelentheti azt, hogy nagyobb valószínűséggel fordulhatnak elő Önnél fertőzések. Lehetséges, hogy kezelőorvosa a Thalidomide BMS-kezelés alatt ellenőrzi majd a vérképét.
Gyakori mellékhatások (10 beteg közül legfeljebb 1 betegnél fordulhatnak elő):
- gyomorrontás, hányinger, hányás, szájszárazság,
- bőrkiütés, száraz bőr,
- a fehérvérsejtek számának csökkenése (neutropénia), amelyet láz és fertőzés kísér.
- a vörösvértestek és fehérvérsejtek, valamint a vérlemezkék számának egyidejű csökkenése (páncitopénia), gyengeség, ájulás vagy bizonytalanságérzés, kimerültség, alacsony vérnyomás,
- láz, rossz közérzet,
- görcsrohamok
- szédülés ("forog a világ" érzés), amely nehézséget okoz a felállás és a mozgás során,
- homályos látás,
- mellkasi fertőzés (tüdőgyulladás), tüdőbetegség,
- lassú szívverés, szívelégtelenség,
- depresszió, zavartság, hangulatváltozások, szorongás,
- halláskárosodás vagy süketség,
- vesebetegség (veseelégtelenség).
Nem gyakori mellékhatások (100 beteg közül legfeljebb 1 betegnél fordulhatnak elő):
- a tüdőben a hörgők gyulladása és duzzanata (hörghurut),
- a gyomornyálkahártya-sejtek gyulladása,
- a vastagbélen keletkező lyuk, amely fertőzést okozhat,
- bélelzáródás,
- vérnyomásesés felálláskor, ami ájuláshoz is vezethet,
- szabálytalan szívverés (szárblokk vagy pitvarfibrilláció), ájulásérzés vagy ájulás.
Nem ismert gyakoriságú mellékhatások (a gyakoriság a rendelkezésre álló adatokból nem állapítható meg):
- elégtelen pajzsmirigyműködés (hipotireózis),
- szexuális funkciózavar, például impotencia,
- a vér súlyos fertőzése (vérmérgezés, szepszis), amely lázzal, hidegrázással és erős remegéssel jár, és esetlegesen alacsony vérnyomással és zavart tudatállapottal (szeptikus sokk) szövődhet,
- tumorlízis szindróma - az anyagcserét érintő szövődmények, amely a daganatos betegség kezelése során fordulhat elő, esetenként akár kezelés nélkül is. Ezt a szövődményet az elpusztuló daganatsejtek bomlástermékei okozzák, és a következő tünetekkel járhat: a vérkép megváltozása; magas kálium-, foszfor- és húgysavszint, valamint alacsony kalciumszint, ami a veseműködés és a szívverés megváltozásához, görcsrohamok kialakulásához és néha halálhoz is vezethet,
- a máj károsodása (májbetegség), a kóros májfunkciós vizsgálati eredményeket is beleértve,
- a gyomorból vagy a belekből származó vérzés (emésztőrendszeri vérzés),
- a Parkinson-kór tüneteinek rosszabbodása (például remegés, depresszió vagy zavartság),
- a has felső részén és/vagy a hátban jelentkező fájdalom, amely erős lehet, és néhány napig tart, esetlegesen hányinger, hányás, láz és szapora szívverés kíséretében - ezeket a tüneteket a hasnyálmirigy gyulladása (pankreátitisz) okozhatja,
- emelkedett vérnyomás a tüdőt ellátó erekben, ami légszomjhoz, fáradtsághoz, szédüléshez, mellkasi fájdalomhoz, szapora szívműködéshez vagy alsó végtagi, illetve bokatáji duzzanathoz vezethet (kisvérköri magasvérnyomás),
- vírusfertőzések, köztük herpesz zoszter (más néven "övsömör", fájdalmas, hólyagos bőrkiütésekkel járó, vírus okozta betegség) és a hepatitisz B-fertőzés kiújulása (ami a bőr és a szem sárgás elszíneződését, sötétbarna színű vizeletet, jobb oldali hasi fájdalmat, lázat és hányingert vagy hányást okozhat),
- olyan agyi állapot, amely látászavarokkal, fejfájással, görcsrohamokkal és zavart tudatállapottal jár, és magas vérnyomás is társulhat hozzá (poszterior reverzibilis enkefalopátia szindróma, rövidítve PRES),
- Bőrelváltozás, melyet a kis erek gyulladása okoz, valamint ízületi fájdalom és láz
(leukocitoklasztikus vaszkulitisz).
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a https://mellekhatas.ogyei.gov.hu/ weboldalon. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Thalidomide BMS-t tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A gyógyszerlevélen és a buborékcsomagoláson feltüntetett lejárati idő ("EXP") után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Ne szedje ezt a gyógyszert, ha sérülést vagy felbontás jeleit látja rajta.
Ez a gyógyszer nem igényel különleges tárolást.
A kezelés végén a fel nem használt kapszulákat vissza kell adnia a gyógyszerésznek vagy a kezelőorvosnak. Ezzel megelőzhető a helytelen felhasználás.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a Thalidomide BMS?
- A készítmény hatóanyaga a talidomid. Minden egyes kapszula 50 mg talidomidot tartalmaz.
- Egyéb összetevők:
-- A kapszula hidegen duzzadó keményítőt és magnézium-sztearátot tartalmaz.
-- A kapszula héja zselatint és titán-dioxidot (E171) tartalmaz.
-- A felirathoz használt festék sellakból, fekete vas-oxidból (E172) és propilén-glikolból áll.
Milyen a Thalidomide BMS külleme és mit tartalmaz a csomagolás?
A Thalidomide BMS fehér, kemény kapszula "Thalidomide BMS 50 mg" jelöléssel. 28 db kapszulát (két buborékcsomagolás, egyenként 14 kapszulával) tartalmazó gyógyszerlevélben kapható.




